II - Mr Hyde : Comment la télomérase peut-elle devenir néfaste pour les Hommes ?
Comme nous l'avons déjà dit, une cellule a un nombre limité de divisions régit par la limite Hayflick qui est la taille minimum que les télomères peuvent atteindre. Normalement, à ce stade, la cellule doit rentrer en sénescence*.
Cependant certaines fois, les cellules continuent de se diviser après avoir atteint cette limite. Nous nous sommes alors demandés pourquoi et quelles sont les conséquences de ces divisions.
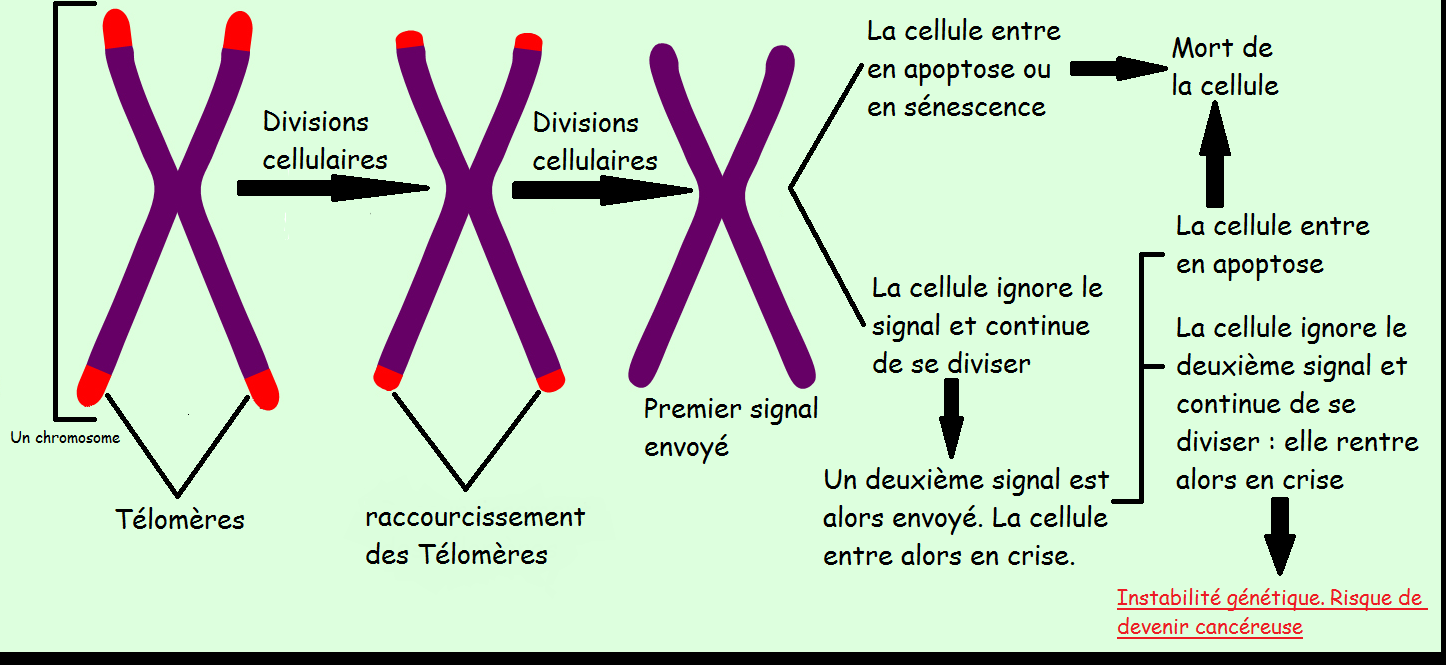
Après avoir franchi la limite de Hayflick et lorsque la shelterine* ne peut plus se fixer sur les télomères, la cellule reçoit un premier signal lui imposant la sénescence réplicative*. Cependant, il arrive que la cellule continue de se diviser et que les télomères continuent de raccourcir jusqu'à ne presque plus exister. L'ADN polymérase* pensera alors que les extrémités des chromosomes sont cassées. Les extrémités vont alors fusionner. Une instabilité génétique apparaît, mais la cellule peut continué de se diviser.
Un nouveau phénomène s'active alors. Une réponse aux dommages de l’ADN (DDR = DNA damage reponse) est activée. Elle envoie un deuxième signal à la cellule. Si ce deuxième message est ignoré ou dysfonctionne, l’instabilité génétique est de plus en plus importante provoquant de nouvelles mutations. La cellule est en crise et peut devenir cancéreuse.
Nous savons également qu'une cellule saine peut subir une mutation. Nous nous demandons comment le phénomène de mutation peut apparaître et quels sont les effets de ce dernier.
La place des nucléotides* est importante car c'est la séquence de nucléotides qui définit le gène. Si un nucléotide est modifié, cela peut entraîner une modification complète du "message" du gène et donc donner un allèle* différent. Cette modification du gène est une mutation.
Les mutations peuvent être dûes à une erreur de réplication de l'ADN polymérase. En effet, celui-ci peut soit oublier une paire de nucléotides (délétion), soit rajouter une paire de nucléotides (addition), soit remplacer un nucléotide par un autre (substitution).
Les mutations génétiques sont spontanées et rares. Cependant, certains facteurs sont capables de modifier un gène en provoquants une mutation : ce sont les agents mutagènes*. Ils sont capables de modifier la composition moléculaire des nucléotides ainsi que celle de l'ADN. En Australie, la population est beaucoup plus assujettie au cancer de la peau car il y a un trou dans la couche d'ozone qui laisse passer les UV émis par le soleil et qui attaquent les cellules de l'epiderme.
Ces derniers ont la capacité de créer des liaisons covalentes* entre deux nucléotides consécutifs. Deux molécules de thymine (T) vont, sous l'influence des UV, créer une dimère* de thymine T=T. Lors de la réplication, l'ADN polymérase ne va pas '"comprendre" cette liaison covalente. Cela créera une modification du gène et par conséquent une mutation de l'ADN.
Heureusement, certains systèmes enzymatiques (protéine de régulation* de l'ADN) sont capables de vérifier les brins d'ADN et ainsi de réparer les erreurs. Il existe une douzaine de protéines capables de faire cela comme p53 ou p16. Elles vérifient tout d'abord l'ADN, puis quand elles ont découvert une erreur, deux chemins s'imposent. Soit l'enzyme répare l'ADN et la cellule reprend ses cycles cellulaires. Soit l'erreur est trop importante et l'enzyme oblige la cellule à entrer en apoptose. La cellule meurt.
Cependant, si la mutation apparaît sur un gène codant pour une protéine de régulation* et que la mutation n'est pas détectée ou si, comme nous l'avons dit précédemment, la cellule continue de se diviser au-delà de la limite de Hayflick, la cellule peut survivre. Elle devient alors un clone cellulaire*. La cellule donne après de multiples divisions plusieurs cellules filles portant la même mutation dans leur ADN. Certaines de ces mutations peuvent donner une cellule cancéreuse*.
Nous nous cherchons à comprendre comment une cellule pourrait devenir cancéreuse.
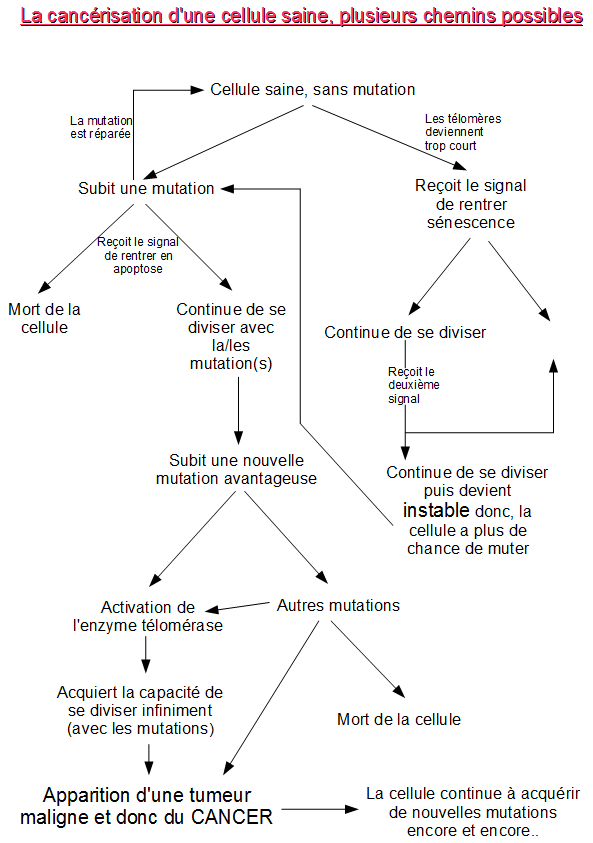
Après avoir évité la vérification par p53, p16..., la cellule devient un clone. Pour survivre, elle a besoin de nouvelles mutations avantageuses. Il y a quatre mutations principales : la capacité à se diviser rapidement, la résistance aux facteurs extérieurs, la possibilité de migrer vers d'autres organes et celle qui permet à la cellule de pouvoir devenir immortelle. Pour cela, l'activation du gène codant pour la télomérase est primordiale (voir introduction pour comprendre le principe de la télomérase). Après plusieurs mutations, les cellules filles deviennent "surpuissantes". Une tumeur* peut se développer.
Les cellules prolifèrent alors et continuent de se développer de façon anarchique, rapidement et un grand nombres de fois. A partir d'un certain stade, la tumeur crée des vaisseaux la reliant avec le système sanguin. Elle peut alors migrer pour pouvoir évoluer à différents endroits et former des métastases*.
Nous nous sommes demandés en quoi la télomérase peut-elle être un avantage pour les cellules cancéreuses.
Si la télomérase n'était pas active, les cellules ne pourraient se diviser qu'un nombre réduit de fois. En effet, comme la télomérase est capable de rajouter des séquences de nucléotides afin de stabiliser la longueur des télomères. Sans elle, la cellule ne pourrait survivre indéfiniment. Au terme de plusieurs divisions sans télomèrase, la cellule deviendrait de plus en plus instable et finirait par mourir. La télomérase est donc primordiale pour la prolifération du cancer.
Le cancer est une maladie difficile à traiter du fait de l'immortalité des cellules, de leurs rapides proliférations, de leurs capacités à ce déplacer et de leurs résistances. Ainsi sans l'enzyme télomérase, les cellules cancéreuses ne pourrait proliférer.
Si nous sommes capables d'inhiber la télomérase ou du moins de la rendre défectueuse dans les cellules cancéreuses, nous serions peut-être capable de détruire ou au moins ralentir le cancer.
